Роль гормонов белковой природы в человеческом организме
Содержание:
Основные функции жиров. Роль и функции жиров в организме человека
Жирами принято называть группу простых липидов, способных утилизироваться организмом человека, имеющих общие структурные особенности. Жиры, некоторые липиды, их составные части ответственны за многие процессы нормальной жизнедеятельности человека. Функции жиров в организме человека очень важны
Функции жиров в организме человека
Физиология, медицина, биохимия интенсивно развиваются параллельно с появлением новых приборных возможностей исследования. Постоянно появляются дополнительные научные данные, с учетом которых основные функции жиров в организме можно представить в предлагаемой совокупности.
Энергетическая . В результате окислительного расщепления из 1 гр жира опосредованно образуется 9 ккал энергии, что значительно превышает аналогичные цифры для белков и углеводов.
Регуляторная . Установлено, что в результате обменных реакций 1 гр жира в организме синтезируется 10 гр «внутренней» воды, которую правильнее называть эндогенной. Вода, которую мы получаем с пищей, напитками, называется «внешней», экзогенной. Вода – интереснейшее вещество, склонное объединяться в группы – ассоциаты. Этим отличаются характеристики воды, претерпевшей таяние, очистку, кипячение. Аналогично отличаются качества воды, синтезировавшейся в организме и поступившей извне. Эндогенная вода синтезироваться должна обязательно, хотя ее роль окончательно пока не установлена.
Структурно-пластическая . Жиры, самостоятельно либо в комплексе с белками, углеводами, участвуют в образовании тканей. Важнейшее значение имеет слой клеточных оболочек, состоящий из липопротеидов – структурных образований из липидов и белков. Нормальное состояние липидного слоя мембраны клетки обеспечивает обмен веществ и энергии. Так структурно-пластические функции жиров в клетке интегрируется с транспортной функцией.
Защитная . Подкожный слой жира выполняет теплосохраняющую функцию, защищает организм от переохлаждения. Это хорошо заметно на примере купающихся в прохладном море детей. Малыши с незначительным слоем подкожного жира замерзают очень быстро. Дети с нормальной жировой прослойкой могут принимать водные процедуры гораздо дольше. Естественный жировой слой на внутренних органах защищает их в некоторой степени от механических воздействий. Незначительная жировая прослойка покрывает в норме многие органы.
Обеспечивающая . Натуральные жиры – это всегда смеси, содержащие дополнительные биологически активные вещества. Роль жиров в организме заключается в параллельном обеспечении важными для физиологии компонентами: витаминами, витаминоподобными соединениями, стеринами, некоторыми сложными липидами.
Косметически-гигиеническая . Тонкий слой жиров, имеющийся на коже, придает ей упругость, эластичность, защищает от растрескивания. Цельность кожи, не содержащей микротрещины, исключает попадание микробов.
Гиперплазия мышц[править | править код]
Отличие гипертрофии от гиперплазииГиперплазия
(новолат. hyperplasia; др.-греч. ὑπερ- — сверх- + πλάσις — образование, формирование) — увеличение числа структурных элементов мышечной ткани (мышечных волокон) путём их деления. В отличие от гиперплазии, гипертрофия предполагает увеличение объемов клеток и саркоплазматических структур, без выраженного деления (новообразования ядер).
Исследования подтверждают, что вклад гиперплазии в объем мышцы составляет менее 5% и носит более существенный характер только при использовании анаболических стероидов. Также гиперплазию могут вызывать блокаторы миостатина. Гормон роста при этом не вызывает гиперплазии.
Люди склонные к гипертрофии обычно имеют большее количество мышечных волокон. Общее число волокон предопределяется генетически и практически не меняется в течение жизни без применения специальной фармакологии. Не доказано увеличения количества мышечных волокон (гиперплазии мышечных волокон) у человека под влиянием силовой тренировки, хотя у животных (млекопитающих и птиц) гиперплазия мышечных волокон возможна.
Исследования
В то время как при гипертрофии мышц наблюдается увеличение количества ядер в мышечной клетке, при исследованиях процессов атрофии на животных было отмечено противоположное явление. Уменьшение количества ядер происходит в результате атрофии мышечных волокон после перерезки спинного мозга, при длительном пребывании в условиях невесомости или временного обездвиживания задней конечности. Таким образом, изменение количества ядер на мышечную клетку, по-видимому, имеет большое значение для регуляции размера клеточной фибриллы. В то же время необходимо иметь в виду, что увеличение количества ядер в мышечном волокне будет происходить до тех пор, пока активность превращения уже существующих ядер окажется способной для обеспечения роста их количества. Действительно, заметные изменения количества ядер в мышечном волокне наблюдались в мышцах, гипертрофированных более чем на 26 %, но не в гипертрофированных на 6,8—15,5 %.
Поскольку ядра дифференцированного мышечного волокна неспособны делиться, основным источником новых ядер в гипертрофированных мышечных волокнах являются миосателлитоциты или клетки-спутники. Миосателлитоциты расположены между базальной пластиной и плазматической мембраной мышечных волокон, для них характерно высокое ядерно-цитоплазматическое соотношение, хорошо развитый аппарат Гольджи, выраженный гранулярный эндоплазматический ретикулум и гетерохроматинизированное ядро. Активация клеток-спутников может происходить под воздействием ряда стимулов, после чего они начинают активно делиться. После этого образовавшиеся в результате митоза дочерние клетки сливаются с расположенными рядом дифференцированными мышечными клетками, обеспечивая таким образом увеличение количества ядер. Роль образующихся при делении миосателлитоцитов ядер в процессе мышечной гипертрофии подтверждается также экспериментами на животных моделях, демонстрирующими, что для обеспечения роста мышц необходимы активация и последующая пролиферация клеток-спутников.
Показано, что параллельно с гипертрофией мышц интенсивная силовая тренировка индуцирует существенное увеличение количества клеток-спутников в скелетных мышцах. Сообщалось об увеличении на 46 % доли миосателлитоцитов в скелетной мышце молодой женщины после 10 недель силовой тренировки. Не так давно увеличение количества миосателлитоцитов было обнаружено в скелетных мышцах группы мужчин в возрасте 70—80 лет, занимавшихся тренировкой выносливости. Таким образом, клетки-спутники обеспечивают увеличение количества ядер в мышечном волокне и возобновление своего собственного пула. Вновь сформированные мышечные волокна замещают поврежденные или вносят свой вклад в гиперплазию мышечных волокон, только если количество вновь сформированных волокон превышает количество волокон, поврежденных во время тренировки.
Ионы кальция:
Кальций отличается тем, что он не
превращается в клетке. Его действие
связано с изменением конформации в
клетках содержание кальция 10-7
моль/л. Вне клеточной жидкости 10-3
моль/л.
В клетку кальций поступает по кальциевым
каналам.
Из клетки удаляется Са-АТФ-азой.
В клетке кальций может депонироваться
в матриксе митохондрий, а в мышечной
ткани в цистернах саркоплазматического
ретикулума (СПР).
Кальций в клетке связывается с белком
кальмодулином (кальмодулин – Молекулярная
масса равна 17000). Связывает кальций в
четырех участках. При этом изменяется
его конформация и он может влиять на
активность ферментов (активирует
кальций-зависимые протеинкиназы).
Продукты превращения инозитолфосфотидов:
В клетках мембран имеются
под действием гормонов активируется
фосфолипаза С и отщепляется инозитолдифосфат
или инозитолтрифосфат. (фосфорелирование
инозитола так же происходит под влиянием
гормонов.
Инозитолтри (ди) фосфат способствует
поступлению кальция в клетку и активации
кальций-зависимых протеинкиназ.
Диацилглицерол, так же активирует
кальций-зависимые протеинкиназы.
Действие гормонов проникающих в
клетку.
К этой группе относятся стероидные и
тиреоидные гормоны. Их рецепторы
локализованы в цитоплазме клеток.
Рецепторы связываются с гормонами и
образуют рецепторно-гормональный
комплекс, который легко проходит в ядро
и связывается с негистоновыми белками.
Происходит активация протеинов
транскрипции (синтез и-РНК) и-РНК поступает
к рибосомам и стимулируется синтез
белка.
Таким образом действие всех гормонов
сводится к следующим механизмам:
-
влияние на количества белка и ферментов.
(гормоны проникают в клетку не проникающие
в клетку, через фосфорелирование ядерных
белков и белков рибосом). Через изменение
скорости распада белков. -
влиянию на активносить ферментов.
Гормоны не проникающие в клетку через
фосфорелирование ферментов (активация
или инактивация). -
влиянию на проницаемость мембран:
-
изменение конформации рецепторной
субъединицы при связывании с гормоном. -
Фосфорелирование белков мембраны.
-
Активация синтеза белков переносчиков
в мембране. -
Включение стероидных гормонов в
мембрану клеток и влияние на свойства
липидного бислоя.
Механизмы прямой и обратной связи в
регуляции синтеза и действия гормонов:
Все железы эндокринной системы
взаимосвязаны механизмами рямой и
обратной связи.
Трансгипофизарный путь прямой связи:
Сигналы из окружающей среды и внутренней
среды организма поступают в ЦНС, где
анализируются импульсы. Из ЦНС поступают
в гипоталамус, который вырабатывает
гормоны либерины и статины влияющие на
выработку трипных гормонов гипофиза.
Они стимулируют синтез гормонов в
периферических железах. Гормоны влияют
на обменные процессы в тканях мишенях
и образуются метаболиты.
Кроме этого есть парагипофизарный
путь прямой связи, когда импульсы из
ЦНС идут в периферическую железу и
стимулируется выработка гормонов,
который оказывает эффект.
Обратная связь: гормоны периферических
желез тормозят образование гормонов
гипофиза, гипоталамуса, кроме этого
существует метаболитная обратная
связь, когда сами метаболиты тормозят
выработку гормонов периферических
желез, гипофиза, гипоталамуса.
ЦНС
↓
парагипофизарный путь
–
–
––– гипоталамус –––
↓ ↓
либерины (+) статины (-)
+
–
–
гипофиз
↓
тропные гормоны
↓ (+)
периферические
эндокринные железы
↓
гормоны
↓
ткани-мишени
↓
метаболиты
Гормоны
гипоталамуса: в гипоталамусе
вырабатывается 2 типа веществ (либирины
– стимулирующие выработку гормонов
гипофиза и статины – угнетающие выработку
этих гормонов)
Либерины статины
Тиролиберин
Соматолибирин соматостатин
Кортиколиберин
Фоллиберин
Люлибирин
Пролактолиберин пролактостатин
Меланолиберин меланостатин
Эти гормоны былди выделены изучены в
70 гг. все эти гормоны пептиды – группа
гормонов не проникающих в клетку.
Действующие по аденилатциклазному
механизму. Мишенью для них являются
клетки передней доли гипофиза. Образуется
ц-АМФ, активируется ПК. Они фосфорилируют
белки рибосом (и происходит синтез
белков – гормонов гипофиза) и белков
мембран (увеличивается их проницаемость
и выход гормонов в кровь).
Тиролиберин – стимулирует синтез
тиротропина и используется для
дифференциальной диагностики при
недостаточности функции щитовидной
железы.
Фолилюбирины: стимулирует выработку
фолликулостимулирующего (ФСГ) и
лютеинизирующего (ЛГ) гормонов гипофиза.
Используется для дифференциальной
диагностики причин бесплодия.
Соматостатин: используется для
лечения больных акромегалией.
Гипоталамус и гипофиз
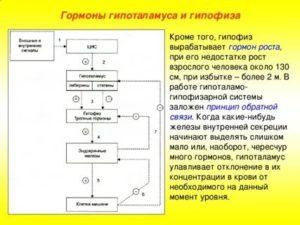
Эндокринная система состоит из группы желез внутренней секреции. Деятельностью этих желез управляют две железы – гипоталамус и гипофиз . Они вырабатывают и выбрасывают в кровь гормоны – химические вещества , влияющие на метаболизм , развитие организма и рост, а также деятельность различных органов и тканей .
СТРОЕНИЕ ЭНДОКРИННОЙ СИСТЕМЫ
Гипоталамус. Является отделом головного мозга, объединяющим нервную систему с эндокринной, отдел регулируюет работу гипофиза, а через него происходит и контроль работы всей эндокринной системы.
Гипофиз. Занимается выработкой гормонов, оказывающих прямое воздействие на ткани организма. Также именно гипофиз контролируют работу других желез эндокринной системы.
Щитовидная железа. Занимается выработкой гормонов, стимулирующих метаболизм организма, гормонов необходимых для умственного развития детей и их физического роста.
Околощитовидные железы. Занимаются выработкой гормонов, принимающих участие в регуляции уровня фосфора и кальция в крови.
Поджелудочная железа. Занимается выработкой гормонов, регулирующих концентрацию глюкозы в крови, а также контролирующих её метаболизм.
Яичники. Женские органы, занимаются выработкой эстрогена и прогестерона — гормонов, контролирующих деятельность женской половой системы и развитие вторичных половых признаков.
Яички. Мужские органы, вырабатывающие тестостерон – гормон, контролирующий развитие вторичных половых признаков у мужчин.
Гипоталамус и гипофиз — два небольшие органа, они находятся у основания мозга и имеют анатомическую связь: с одной стороны, некоторые нейроны гипоталамуса имеют удлинения, которые достигают задней доли гипофиза (нейрогипофиза); с другой стороны, сеть венозных сосудов, или портальная система, переносит гормоны, выработанные гипоталамусом, к передней части гипофиза (аденогипофизу).
Также эта маленькая железа контактирует с различными зонами нервной системы и поэтому может получать множество стимулов, как физических, так и психических, но особенно важна, поскольку регулирует деятельность эндокринной системы.
Эта железа контролирует деятельность внутренних органов и действует согласно различным нуждам организма.
Гипофиз регулирует деятельность эндокринной системы с помощью вырабатываемых им гормонов, которые действуют на ткани органов и на другие железы, входящие в состав эндокринной системы.
Помимо этого он накапливает и высвобождает в нужный момент гормоны, вырабатываемые гипоталамусом, — антидиуретический гормон и окситоцин. Подробнее о гипофизе в ст.”Строение гипофиза”.
ГОРМОНЫ ГИПОФИЗА
Меланоцитстимулирующий гормон;(МСГ)Область действия: Кожа.
Функции: Стимулирует выработку меланоцитов, влияющих на цвет кожи.
Антидиуретический гормон, или вазопрессин (АДГ)Область действия: Почки.Функции: Удерживает воду в почках, регулирует артериальное давление.
Гормон роста, или соматотропин (ГР, СТГ или РГ);Область действия: Весь организм.Функции: Стимулирует рост мышц, костей и органов в детстве и во время полового созревания.
Тиреотропин (ТТГ) Область действия: Щитовидная железа.Функции: Стимулирует деятельность щитовидной железы.
Адренокортикотропин (АКТГ)Область действия: Надпочечники.Функции: Стимулирует выработку кортикостероидов надпочечными железами.
Пролактин (ЛТГ) Область действия: Грудь.Функции: Провоцирует выработку молока грудными железами после родов.
Гонадотропины•;Фолликулостимулирующий гормон (ФСГ)•;Лютеинизирующий гормон, или гормон, стимулирующий интерстнциальные клетки (ЛГ или ГСИК)Область действия: Гонады (яйцеклетки и яички).Функции: Регулирует созревание сперматозоидов и яйцеклеток, а также выработку половых гормонов.
Сульпирид
По клинико-фармакологической группе относится к антипсихотическим препаратам. По фармако-терапевтической группе относится к нейролептическим антипсихотическим средствам.
Сульпирид характеризуется блокадой преимущественно допаминовых рецепторов. На адренергические, серотониновые, гистаминовые, холинергические ГАМК (GABA) практически не влияет. Отсюда имеет меньше побочных эффектов (по сравнению с хлорпромазином и другими препаратами группы).
Сульпирид
Сульпирид обладает следующими действиями на организм человека:
- антипсихотическое (суточная доза более 600 мг);
- стимулирующее выработку пролактина;
- антиэметическое (противорвотное за счет блокады рвотного центра);
- антидепрессивное (суточная доза менее 600 мг);
- снижает абдоминальные боли и психосоматику при ЯБЖ, язве 12-перстной кишки, СРК;
- лечит головокружение (различной этиологии – ЧМТ, отит, невриты и др.).
Сульпирид был показан как лекарство с потенциальным эффектом галактопоэза, когда у женщин наблюдалось повышение сывороточного пролактина.
Имеются несколько клинических исследований, которые подтверждают его эффективность в отношении стимуляции лактации. В одно из них вошли 130 первородящих женщин: 66 получали сульпирид в дозе 50 мг перорально каждые 12 часов в течение 7 дней, а 64 были в группе плацебо. В результате лечения уровень пролактина в сыворотке крови увеличился, как и секреция молока.
В предыдущем исследовании сообщалось об эффективной пероральной дозе сульпирида 50 мг каждые 8 часов в течение 4 недель для лечения женщин с гипогалактией. При этом концентрации пролактина в сыворотке крови увеличивались в течение первых 2 недель, в то время как в контрольной группе снижались. Причем, после 28 дней лечения сульпиридом, младенцы от матерей, получавших лечение, демонстрировали более высокую прибавку в весе, чем в группе плацебо. Эти результаты были подтверждены другими исследованиями.
Период полувыведения сульпирида из плазмы у человека – 7,15 часа. Выводится почками практически (95%) в неизменном виде.
Среди побочных эффектов у кормящих женщин были:
- головная боль;
- усталость;
- экстрапирамидные симптомы (редко);
- острые дистонические реакции;
- эндокринные нарушения.

Усталость
Препарат в целом переносится хорошо, выраженность и частота нежелательных реакций меньше по сравнению с хлорпромазином. Но только врач принимает решение о возможности его применения у беременной и кормящей исходя из индивидуального анамнеза и оценив пользу и риски.
Сульпирид обычно используется в различных странах, включая Зимбабве, Южную Африку и Чили. В первую очередь сульпирид используется при шизофрении (это антипсихотик и антидепрессант), но он также увеличивает уровень пролактина в сыворотке и, таким образом, может увеличить удой грудного молока.
Гипофиз и эпифиз

В предыдущей статье мы обсудили гипоталамус и гипофиз, которые теснейшим образом связаны друг с другом. Гипоталамус выделяет либерины и статины, регулирующие деятельность гипофиза. Сейчас мы подробнее познакомимся со строением гипофиза и гормонами, которые он выделяет.
Гипофиз
Гипофиз (нижний мозговой придаток, питуитарная железа) – железа внутренней секреции, расположенная в основании черепа. Состоит из трех долей: передней, промежуточной (средней) и задней. Гипофиз называют “дирижером” желез внутренней секреции, так как его гормоны влияют на их работу.
В передней части гипофиза (аденогипофиз) вырабатываются и выделяются в кровь тропные (от греч. tropos — направленность) гормоны:
- Тиреотропный гормон (ТТГ) – стимулирует выделение гормонов щитовидной железой (лат. glandula thyroidea – щитовидная железа)
- Адренокортикотропный (АКТГ) – стимулирует кору надпочечеников (от лат. adrenalis – надпочечный и лат. cortex – кора)
- Гонадотропный (ГТГ) – влияет на секрецию половыми железами половых гормонов и на созревание в половых железах яйцеклеток/сперматозоидов (лат. gonas – половая железа)
- Соматотропный (СТГ) – гормон роста, оказывает влияние на рост и развитие всех клеток организма (греч. soma – тело)
- Пролактин – стимулирует развитие молочных желез и образование в них молока у кормящих матерей
Особенное внимание обратим на гормон роста – СТГ. Нарушение его секреции приводит к тяжелым заболеваниям, так как он влияет на рост и развитие организма
Секреция СТГ может быть повышена, в этом случае говорят о гиперфункции аденогипофиза (греч. hyper – над), или снижена, в таком случае говорят о гипофункции аденогипофиза (греч. hypo — внизу).
В детском и во взрослом возрасте последствия гипо- и гиперфункции отличаются.
https://youtube.com/watch?v=MNk2PLsRXJM
При гиперфункции аденогипофиза (СТГ повышен) в детском возрасте происходит избыточный рост костей и развивается гигантизм, пропорции тела при этом сохраняются. При гигантизме рост человека может достигать 2 и более метров. При такой патологии наиболее предрасположены к заболеваниям половые железы, суставы, нередко нарушается психика.
Во взрослом возрасте гиперфункция аденогипофиза не сопровождается увеличением роста, так как рост большей части костей окончен.
Однако, начинают избыточно расти те кости, в которых есть хрящевая прослойка: фаланги пальцев, нижняя челюсть. Утолщаются губы и нос, увеличиваются внутренние органы.
При гипофункции аденогипофиза (снижена секреция СТГ) в детском возрасте развивается карликовость – задержка роста. При карликовости тело имеет правильные пропорции, рост не более 1 метра, психика в норме. Это состояние может корректировать врач, вовремя (в детстве!) назначив гормон роста в виде лекарства.
При гипофункции аденогипофиза во взрослом возрасте развивается изменение обмена веществ, что может привести как к истощению, так и к ожирению.
Промежуточная доля гипофиза синтезирует и выделяет меланотропный (меланоцитостимулирующий гормон). Вам уже известно, что меланоциты располагаются в базальном слое эпидермиса, их пигмент – меланин, придает темную окраску коже. Меланотропный гормон стимулирует активность меланоцитов: они синтезируют меланин, пигментация кожи усиливается.
Вазопрессин усиливает реабсорбцию (всасывание) воды в канальцах нефрона, тем самым снижая выведение ее с мочой. При нарушении секреции АДГ объем мочи может возрастать до 20 литров в сутки! Такое состояние носит название несахарный диабет, так как подобно диабету характеризуется увеличением диуреза (объема мочи) и сильной жаждой.
Окситоцин играет важную роль во время родов – он стимулирует сокращения матки, способствую продвижению плода по родовым путям. У кормящих матерей окситоцин способствует лактации (секреции молока) в молочных железах при кормлении.
Эпифиз
Эпифиз (шишковидное тело) – эндокринная железа внутренней секреции, анатомически относящаяся к промежуточному мозгу. В зависимости от освещенности, нейроны эпифиза синтезируют и выделяют гормон мелатонин, участвующий в регуляции суточных и сезонных ритмов организма. Свет тормозит выработку мелатонина.
Секреция
Гормоны секретируются в кровь путем простой диффузии (стероиды), экзоцитоза (инсулин, глюкагон, прол актин, СТГ) или путем превращения нерастворимых предшественников в растворимые продукты (Т4 и Т3).
Поскольку запасающая способность эндокринных клеток ограничена, скорость секреции большинства гормонов соответствует скорости их синтеза. При этом гормоны аденогипофиза повышают как скорость синтеза, так и скорость секреции гормонов желез-мишеней. Если гормон запасается в секреторных гранулах, то вслед за выбросом гормона ускоряется его синтез. Этим объясняется двухфазное высвобождение инсулина после инфузии глюкозы. Скорость секреции многих гормонов регулируется нервной системой, зависит от возраста и различается во время сна и бодрствования, причем изменения скорости секреции пропорциональны изменениям скорости синтеза.
Секреция гормонов может быть ритмической, с периодом от минут до часов (ультрадианный ритм), около суток (циркадианный ритм) или месяцев и даже лет (инфрадиан-ный ритм). Например, выбросы ЛГ и ФСГ происходят им-пульсно — каждые 30—90 мин, при этом амплитуда выбросов меняется на протяжении суток. Секреция АКТГ (и кортизола) характеризуется суточным ритмом, а периодичность секреции Т4 и Т3 значительно превышает 24 ч. Не выяснено, какие локальные факторы — изменения скорости синтеза гормона, изменения гемодинамики или другие — влияют на ритм секреции, но задает его в большинстве случаев ЦНС. Не всегда понятно физиологическое значение импульсной секреции, но известно, что от частоты и амплитуды выбросов гормона зависит его действие. Так, многократное введение гонадолиберина (имитирующее импульсную секрецию) стимулирует периодические выбросы ЛГ, а непрерывная инфузия подавляет секрецию Л Г. Изменение частоты или амплитуды ритма секреции гормонов— важный диагностический признак. Например, уже на ранней стадии гипофизарного синдрома Кушинга теряется суточный ритм секреции кортизола, а при нервной анорексии нарушается импульсная секреция гонадолиберина. Кроме того, ритм секреции гормона необходимо учитывать при планировании и оценке результатов лабораторных исследований.
Примеры гормональных иерархических пирамид
Теперь построим несколько иерархических пирамид для внесения большей ясности в понимание принципа работы эндокринной системы человека.
Гормоны щитовидной железы
Ярким примером может послужить влияние вышележащих структур на синтез гормонов щитовидной железы. ЦНС, воспринимая информацию из окружающей среды, посылает нервные импульсы в гипоталамус, где синтезируется тиреотропин — рилизинг-гормон. Рилизинг-гормоны – это гормоны гипоталамуса, которые стимулируют синтез и секрецию тропных гормонов гипофиза. Под влиянием гормона гипоталамуса в гипофизе секретируется ТТГ (тиреотропный гормон), который стимулирует синтез и секрецию трийодтиронина (Т3) и тироксина (Т4).
По данной системе и классифицируют заболевания, связанные с нарушением синтеза и секреции гормонов щитовидной железы. Например, гипертиреоидизм (синдром повышения функции щитовидной железы с избытком ее гормонов) будет называться первичным в случае поражения непосредственно щитовидной железы (орган может быть поражен опухолью или каким-либо еще заболеванием). При первичной патологии щитовидной железы структуры ЦНС, гипоталамуса и гипофиза функционируют правильно, в них нет никаких повреждений. При вторичном гипертиреоидизме будет поражен уже гипофиз, а при третичном имеется поражение гипоталамуса.
Гормоны надпочечников
Кортикотропин – рилизинг-гормон (гормон гипоталамуса) вызывает высвобождение АКТГ (адренокортикотропного гомона) в гипофизе, за счет чего стимулируется секреция гормонов надпочечниками (кортизол, альдостерон и андрогены).
Подобно патологиям щитовидной железы в данном случае так же в зависимости от того, какое звено поражено, так и будет называться патология. При первичном заболевании наблюдается поражение надпочечников, при вторичном — гипофиза, а при третичном — гипоталамуса.
Гормон роста
В регуляции секреции гормона роста участвует два гормона — стимулирующий соматотропин (гормон передней доли гипофиза) и тормозящий соматостатин (гормон гипоталамуса).
Половые гормоны
Для регуляции синтеза и секреции половых гормонов также необходимы гормоны гипоталамуса и гипофиза. Так, гипоталамус синтезирует так называемый гонадотропин – рилизинг-гормон, который, в сою очередь, действует на ткань гипофиза. Там синтезируются лютеинизирующий гормон (ЛГ) и фолликулостимулирующий гормон (ФСГ).
ЛГ вызывает повышение синтеза тестостерона (основной мужской половой гормон).
Тестостерон обладает свойством проходить через гематоэнцефалический барьер (полупроницаемая мембрана в ткани мозга, которая служит защитным механизмом, так как она пропускает через себя лишь некоторые вещества). При этом в мозге он превращается в эстроген, поэтому у мужчин в мозге больше эстрогена, чем у женщин.
У женщин под влиянием ЛГ происходит повышение синтеза и секреции прогестерона (гормон, который регулирует менструальный цикл и беременность), стимулируется овуляция и формирование желтого тела.
ФСГ стимулирует образование спермы у мужчин и рост фолликулов (область, в которой содержится яйцеклетка) в яичниках у женщин.
Пролактин – это гормон гипофиза, который отвечает за развитие молочных желез у женщин и образование молока в период грудного вскармливания. Согласно иерархической системе регуляции, в гипоталамусе секретируется гормон, тормозящий действие пролактина на организм, известный как пролактостатин (пролактин-ингибирующий фактор или ПИФ).
11.Понятие о каскадном механизме усиления и подавления гормонального сигнала.
Каскадный
механизм усиления и подавления
сигнала. Передача
сигнала от мембранного рецептора через
G-белок на фермент аденилатциклазу
служит примером каскадной системы
усиления этого сигнала. Одна молекула,
активирующая рецептор, может «включать»
несколько G-белков, и затем каждый
активирует несколько молекул
аденилатциклазы с образованием тысяч
молекул цАМФ. На этом этапе сигнал
усиливается в 102-103 раз.
Образующийся цАМФ «включают» другой
фермент — протеинкиназу А, усиливая
сигнал ещё в 1000 раз. Фосфорилирование
ферментов протеинкиназой А ещё больше
усиливает сигнал, в результате суммарное
усиление равно 106-107 раз.
Таким образом, по механизму каскадного
усиления одна молекула регулятора
способна изменить активность миллионов
других молекул.